Veeva Vault Registrations
規制の変更に速やかに対応
グローバルな製品登録および関連する変更を追跡します
Announced 2015
Status MATURE
Customers 100+
Vault Registrationsにより、スポンサーはグローバルな製品登録の計画、追跡、レポートと、規制当局とのやり取りやコミットメントの管理を行えます。
イベント機能を使用して、変更案の初回評価を終えてから提出書類を作成するまでに行われた製品の変更、規制当局とのやり取り、最終的な登録の更新を管理できます。
ラベルの変更はグローバルでもローカルでも追跡・管理できます。また、RegistrationsはEUの規制に準拠する製品データ出力(xEVMPDおよびIDMPなど)にも対応しています。
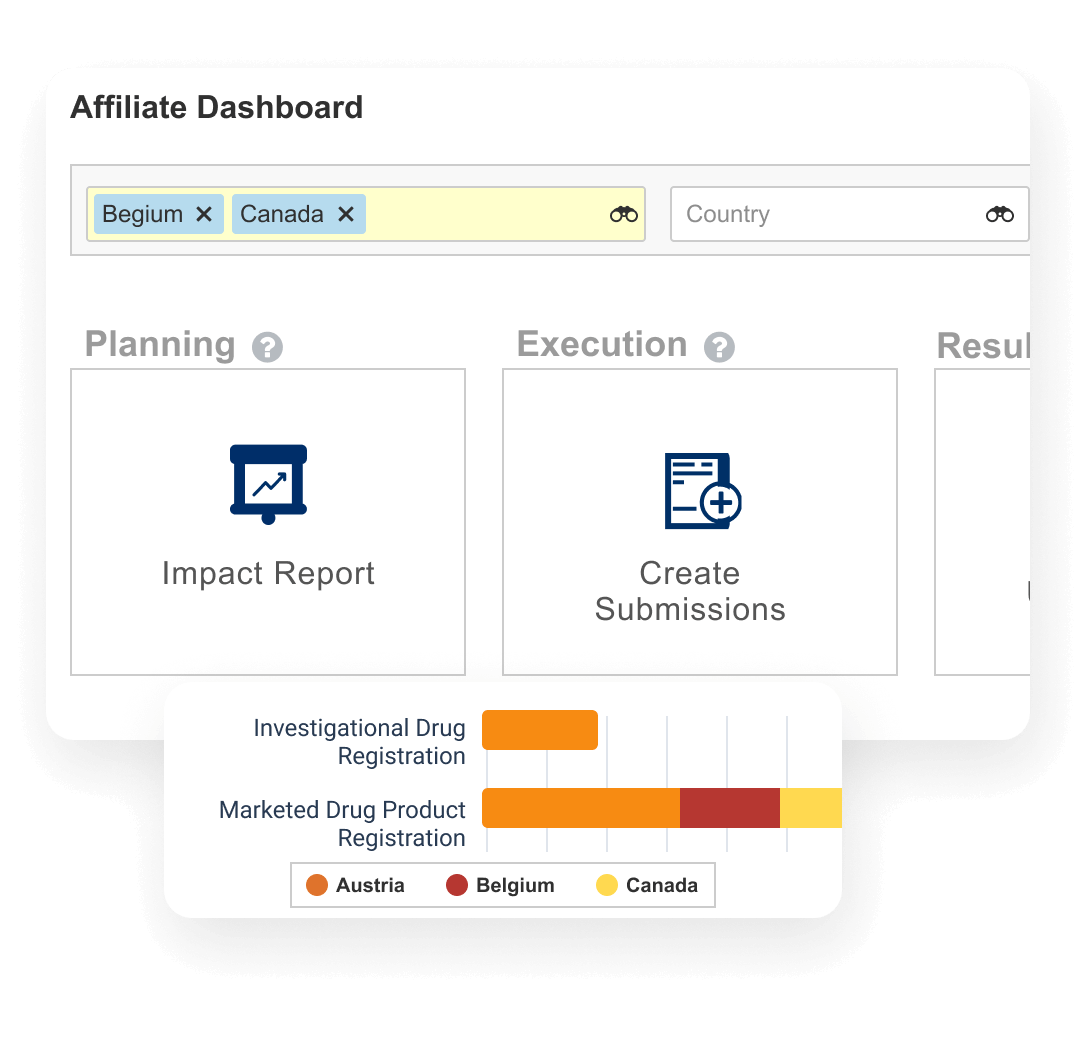
ダッシュボードとレポートにより、変更イベントの進捗状況を追跡し、各国の製品登録情報を把握できます。
Vault Registrationsが選ばれる理由
製品登録の計画、追跡、
レポート
データ品質の向上
データの重複や不一致を減らして、登録管理を効率化します。グローバルな可視性
グローバルな製品ポートフォリオの販売承認状況を完全に可視化し、常に最新の情報を提供します。規制当局への対応を迅速化
製品登録に関する問い合わせやコミットメントを管理し、回答の期限を遵守することができます。
予想を超える
成果を実現
15社
大手製薬企業22社のうちVault RIMを使用している企業の数
88件
統合されたITシステムの数
90%
標準作業手順書の削減率











